桂林医学院第二附属医院药物临床试验机构成立于2018年7月,葛波院长担任药物临床试验机构主任,夏中华副院长担任药物临床试验机构副主任;下设药物临床试验机构办公室,黄桂红担任办公室主任,主持具体工作。根据《医疗器械临床试验机构条件和备案管理办法》,2018年10月,我院在“医疗器械临床试验机构备案管理信息系统”完成14个医疗器械专业组备案(备案号:械临机构备201800309),包括呼吸与危重症科、妇科、心血管内科、胃肠外科、内分泌科、泌尿外科、血液内科、肿瘤内科、肾内科、检验科(含5个专业)。现专业研究团队约200人均参加GCP培训并考试合格,取得GCP证书,建立起一支高水平、高素质的药物临床试验人才队伍。医院具有完善的临床试验基础设施和人员配备,另设有独立的药物临床试验伦理委员会。
机构在秉承真实性、科学性、伦理性、可靠性的原则上,遵循药物临床试验质量管理规范(GCP)和相关法律法规的基础上,针对GCP相关知识培训、临床试验的质量控制、管理制度修订、SOP的规范和可操作性等方面,形成一套完善的质量控制管理体系。
医院临床试验机构现可承担医疗器械和体外诊断试剂的注册临床试验以及研究者或申办方发起的上市后临床研究。
主要业务范围:
1.医疗器械和体外诊断试剂的注册临床试验和上市后临床研究。
2.其他相关业务。
联系方式:
| 项目接洽人 |
黄桂红 0773-5582091 |
| 机构电话 |
0773-5590035 / 18593234093 |
| 机构邮箱 |
glyxydefsyygcp@163.com |
| 机构传真 |
0773-5590035 |
| 接待时间段 |
周一至周五 上午:08:00 - 12:00 下午:14:30 - 17:30 |
| 办公室楼层地址 |
桂林医学院第二附属医院门诊楼6楼药物临床试验机构办公室 |
| 器械备案号 |
械临机构备 201800309 |
| 器械备案专业 |
内科 - 呼吸内科专业 内科 - 心血管内科专业 内科 - 血液内科专业 内科 - 肾病学专业 内科 - 内分泌专业
外科 - 普通外科专业 - 胃肠外科 妇产科 - 妇科专业 肿瘤科 医学检验科 - 临床体液、血液专业/临床微生物学专业/临床化学检验专业/临床免疫、血清学专业/临床细胞分子遗传学专业
|
| 开展项目 |
IV期药物临床试验上市后再评价 医疗器械临床试验 体外诊断试剂临床试验
|
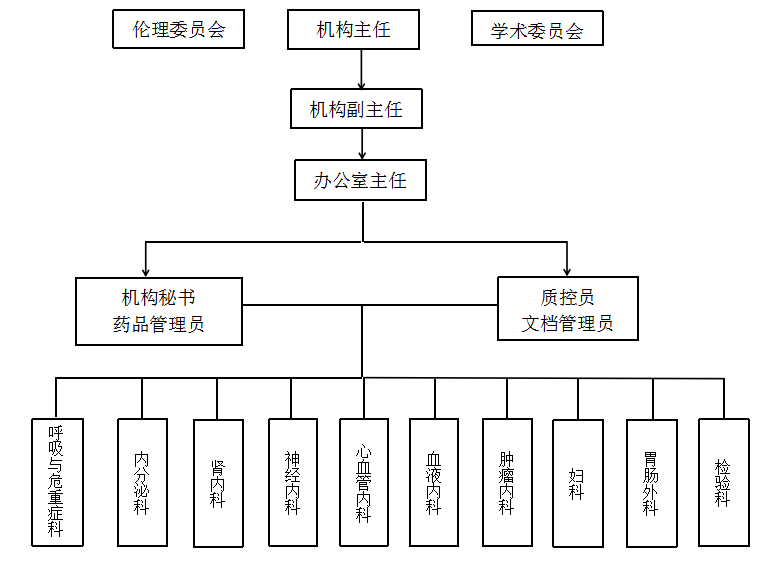
组织机构图:
药物/医疗器械/体外诊断试剂临床试验项目资料递交清单
| 1 |
研究者手册
|
| 2 |
临床试验方案 |
| 3 |
研究病例(样表) |
| 4 |
病例报告表(样表) |
| 5 |
受试者日志(如适用) |
| 6 |
知情同意书(样稿) |
| 7 |
受试者招募广告(样稿) |
| 8 |
伦理委员会批件及成员表(组长单位) |
| 9 |
伦理委员会备案回执(组长单位) |
| 10 |
国家药品监督管理局批件 |
| 11 |
申办者资质证明性文件
|
| 12 |
CRO、SMO资质证明性文件(如适用)及委托书 |
| 13 |
研究者资质(履历表、GCP证书等)及研究小组成员名单 |
| 14 |
试验用药物说明书、药检报告
|
| 15 |
其他文件(如研究保险等)
|

